Арт от вич инфекции
Содержание статьи
Антиретровирусная терапия и ее влияние на здоровье пациентов с ВИЧ — Семейная клиника ОПОРА г. Екатеринбург
Несмотря на прогресс современной медицины в лечении и профилактике ВИЧ-инфекции, по оценкам ВОЗ, в конце 2012 года в мире насчитывалось 35,3 миллиона людей с ВИЧ, из которых 2,3 миллиона составляли случаи новых заражений. Кроме того, более 1 миллиона людей в год умирает от осложнений, связанных с ВИЧ (1). Наиболее быстро ВИЧ распространяется в Восточной Европе, и заболеваемость в Украине остается на достаточно высоком уровне. Именно поэтому главной целью ВОЗ является оптимизация профилактики передачи этого заболевания и существующих методов терапии, а также обеспечение своевременного контроля действенности терапии, минимизации побочных эффектов и повышению, таким образом, общей эффективности лечения(1).
Как действует ВИЧ?
ВИЧ поражает иммунокомпетентные клетки – CD4+-Т-лимфоциты, имеющие также название – «хелперы» (от английского слова «help” –помогать). Именно эта популяция лимфоцитов, несущих на поверхности рецепторы CD4, отвечает на клеточном уровне за иммунный ответ – способность организма эффективно противостоять инфекциям. Вирус постепенно инфицирует все большее и большее количество CD4+-Т-лимфоцитов, а инфицированные ВИЧ клетки гибнут. Соответственно, число CD4+-Т-лимфоцитов в организме снижается, что приводит к нарушению сначала клеточного иммунитета, а потом гуморального иммунного ответа (выработки антител, связывающих чужеродные агенты при их попадании в организм). Далее вирус поражает и другие типы клеток, например, макрофаги, отвечающие за «обезвреживание» инородных агентов, попадающих в организм. В результате нарушается связь между различными типами клеток, лежащая в основе иммунного ответа. Нарастает поражение иммунной системы, которое приводит к заражению больного сопутствующими ВИЧ ( т.н. оппортунистическими) инфекциями – туберкулезом, токсоплазмозом, гепатитом В и другими опасными заболеваниями. На более поздних этапах поражение иммунной системы приводит к развитию злокачественных новообразований и к синдрому приобретенного иммунодефицита (СПИДу) – последней стадии заболевания. При отсутствии лечения у большинства ВИЧ-инфицированных людей пациентов от момента постановки диагноза ВИЧ до развития СПИДа проходит примерно10-15лет(3).
Можно ли вылечить ВИЧ?
Основная сложность борьбы с ВИЧ заключается в сильной изменчивости протеинов (белков), входящих в состав оболочки вируса, из-за которых иммунитет не в состоянии выработать антитела, способные блокировать вирус на выходе из клетки и предотвратить дальнейшее его распространение и гибель популяции Т-лимфоцитов. Поэтому на сегодняшний день не существует лекарства, способного полностью излечить заболевание, хотя достижения современной медицины позволяют надеяться на то, что мир стоит на пороге открытия способа терапии, позволяющего обеспечить полное выздоровление пациента. В 2013г в американском штате Миссисипи был официально зарегистрирован уникальный случай девочки 2,5 лет, которой удалось выздороветь сразу после агрессивного курса лечения, проведенного вскоре после рождения. А ученым Орегонского университета удалось добиться успеха при исследованиях вакцины против ВИЧ на животных – если в 1 фазе исследования препарат помог всего 50% инфицированных обезьян, то во 2 фазе полностью избавились от вируса практически 100% животных. Это говорит о том, что в перспективе возможен путь обезвреживания вируса на том этапе, когда он еще находится в клетке.
Однако на сегодняшний день, когда средства, позволяющего полностью вылечить ВИЧ, не существует, ключевым фактором, от которого зависит прогноз заболевания, является своевременное начало антиретровирусной терапии, которая может практически полностью остановить прогрессирование заболевания и предотвращает дальнейшую передачу вируса (1).
Что такое антиретровирусная терапия (АРТ)?
Антиретровирусные препараты направлены на замедление репродукцию вируса, т.е. на уменьшение его количества в организме. Антиретровирусная терапия (АРТ) существенно замедляет прогресс заболевания именно путем предотвращения репликации вируса и, следовательно, уменьшение концентрации вирусной РНК (известной как «вирусная нагрузка»,или «виремия») в крови пациента. В конце 2012 года антиретровирусную терапию получало 9,7 миллиона человек в странах с низким и средним уровнем дохода. По рекомендации ВОЗ, она применяется лишь после всех необходимых тестов и время ее начала определяет индивидуально лечащий врач (1). Показания к антиретровирусной терапии и оценка ее эффективности основаны на регулярном определении концентрации вирусной РНК (количественном определении РНК ВИЧ) и уровня лимфоцитов CD4. Снижение концентрации вирусной РНК в крови ведет к повышению уровня лимфоцитов CD4 и отдалению развития СПИДа.
Когда следует начинать АРТ?
Независимо от стадии заболевания, АРТ следует назначать всем пациентам, у которых уровень лимфоцитов CD4 составляет >350 клеток/мм3 и ≤ 500 клеток/мм3. АРТ также следует назначать всем пациентам, у которых уровень лимфоцитов CD4 составляет ≤350 клеток/мм3 на поздней и терминальной стадии заболевания ( стадия 3 и 4 по классификации ВОЗ). Если у пациента имеет место сопутствующая инфекция, такая как туберкулез в активной стадии или гепатит В с хронической печеночной недостаточностью, АРТ назначается независимо от уровня лимфоцитов CD4(2).
Какие препараты назначаются в составе АРТ?
Высокоактивная антиретровирусная терапия, согласно рекомендациям ВОЗ 2013г, состоит из одновременного приема трех-четырех сильнодействующих препаратов. Существует три группы антиретровирусных препаратов: нуклеозидные ингибиторы обратной транскриптазы (НИОТ), ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ) и ингибиторы протеазы (ИП)(2).
Согласно рекомендациям ВОЗ, в качестве первой линии АРТ при ВИЧ-инфекции назначаются два препарата НИОТ и один – ННИОТ (тенофовир (TDF) + ламивудин (3TC) или эмтрицитабин (FTC) + эфавиренз (EFV) в фиксированных дозах; при непереносимости данной комбинации, ее недоступности на рынке или противопоказаниях к ней назначаются зидовудин (AZT) + 3TC + EFV, или AZT + 3TC + невирапин (NVP),или TDF + 3TC (or FTC) + NVP.Использование ставудина (d4T) в качестве терапии первой линии не рекомендуется ввиду его серьезных побочных эффектов. В качестве терапии второй линии рекомендуется комбинация двух НИОТ и ИП, усиленных ритонавиром. Общие принципы перехода на терапию второй линии, как и в случае терапии первой линии, основываются на комбинации двух НИОТ в фиксированных дозах: если схема TDF + 3TC (или FTC) оказалась неэффективной, следует использовать схему, основанную на зидовудине и ламивудине (AZT + 3TC), а если эта схема, или схема, основанная на ставудине, при ее применении в качестве терапии первой линии, оказалась неэффективной, то наоборот, следует заменить ее на схему TDF + 3TC (или FTC).Из ингибиторов протеазы рекомендуются атазанавир (ATV) и лопанавир (LPV) в фиксированных дозах. Наконец, режимы терапии третьей линии ВОЗ рекомендует регламентировать национальными протоколами, включая в них препараты с минимальным риском перекрестной резистентности ( устойчивости) вируса к тем препаратам,что уже использовались в схемах терапии первой и второй линии у данных пациентов, если по каким-либо причинам эти схемы пришлось отменить ( из-за плохой переносимости, неэффективности, выраженности побочных эффектов).
Эффективность терапии определяется с помощью клинических исследований через 6-12 месяцев после ее начала. Наиболее достоверным является определение уровня РНК вируса в крови (вирусной нагрузки), но если этот тест не доступен, используется обыкновенное измерение уровня лимфоцитов CD4,по которому можно судить о прогрессе заболевания и эффективности применяемой схемы(2).
Почему соблюдение режима АРТ имеет решающее значение для дальнейшего прогноза пациента?
По данным разных источников, до 50% носителей ВИЧ после двух-трех лет лечения отказываются от терапии, тем самым обрекая себя на скорый прогресс заболевания и ухудшение качества жизни(4). Важно понимать, что лечение ВИЧ является пожизненным, которое нельзя прекращать – иначе возобновление жизненного цикла вируса, который «поднимет голову» вскоре после прекращения терапии, приведет к началу нового витка гибели иммунокомпетентных клеток, ухудшению состояния иммунитета, присоединению новых инфекций и прогрессу заболевания вплоть до развития СПИДа. На самом деле терапия ВИЧ не требует особых изменений в привычном режиме пациента – препараты АРТ обычно принимают один или два раза в день, и пациенты, у которых правильно подобрана схема терапии, очень быстро отлаживают режим их приема. Он ничем не отличается от режимов приема препаратов, принимаемых «здоровой» частью населения – людьми с диабетом, с заболеваниями щитовидной железы, с сердечно-сосудистыми заболеваниями, а иногда и оказывается значительно более простым – недаром пациенты с многолетней историей приема АРТ часто говорят, что пьют эти таблетки, как витамины.
Нельзя пропускать прием таблеток или «забывать» о следующей дозе более чем на 2 часа после стандартного времени приема – статистика показывает, что АРТ эффективна тогда, когда пациент принимает не менее 95% от необходимой дозы всех препаратов(4), что означает, что при приеме 1 раз в день в месяц можно пропустить всего лишь прием одной дозы, а при приеме 2 раза в день – не более 3 приемов!
Кроме того, необходимо помнить о возможных лекарственных взаимодействиях компонентов АРТ с другими принимаемым пациентом лекарственными препаратами. Иногда последние могут усиливать эффект АРТ, а иногда, наоборот, его уменьшать. Эффект лекарственных взаимодействий зависит от фармакокинетики дополнительно принимаемых пациентом препаратов – скорости достижения максимальной концентрации в крови, периода полувыведения, всасываемости в кишечнике. Поэтому не следует начинать прием никаких дополнительных лекарственных средств на фоне АРТ без консультации с врачом-инфекционистом. Даже при приеме обезбаливающих препаратов или растительных средств (фитотерапии) следует предварительно получить консультацию врача. Особенно часто во взаимодействие с другими препаратами вступают ИП и НИОТ. Их действие может ослабевать под действием препаратов, принимаемых для снижения кислотности желудочного сока (например, ингибиторы протонной помпы) или некоторых антибиотиков (макролидов). И наоборот, обычный грейпфрутовый сок может многократно увеличивать эффективность некоторых ИТ (4). Наблюдается также и «обратное» влияние – лекарства, применяемые для АРТ могут снижать эффективность , например, некоторых гормональных препаратов, противозачаточных средств, – последние под влиянием АРТ очень быстро выводятся из организма,- поэтому женщинам, принимающим АРТ, рекомендуется использовать дополнительные методы контрацепции. Некоторые сильнодействующие обезболивающие из группы опиоидов (метадон) также вступают во взаимодействие с препаратами АРТ, вследствие чего может потребоваться увеличение их доз.
Отдельно следует отметить препараты, снижающие уровень холестерин (ХС) в крови(статины), которые некоторые пациенты принимают постоянно. Учитывая, что одним из побочных действий АРТ является увеличение уровня ХС, а также других составляющих т.н. «липидного профиля» ( например, триглицеридов (ТГ), логично предположить, что на фоне АРТ продолжение приема статинов благоприятствует общему состоянию здоровья пациента, снижая уровень ХС. Однако поскольку в организме и статины и препараты АРТ метаболизируются одним и тем же путем, их одновременное применение способствует усилению опасного побочного эффекта статинов – разрушения мышц, или рабдомиолиза. Поэтому при одновременном приеме статинов и препаратов АРТ обязательно необходимо проконсультироваться с врачом.
При приеме препаратов АРТ не следует верить и в распространенный миф о том, что постоянный прием таблеток от ВИЧ вреден и сопряжен с необратимыми токсическими эффектами. Терапия ВИЧ действительно имеет побочные действия, которые, тем не менее, можно минимизировать, а часто и свести к нулю, если соблюдать рекомендации по лечению и проходить необходимые обследования, чтобы врач мог вовремя сориентироваться, какие органы и системы пациента наиболее чувствительны к назначенным препаратам, и купировать имеющиеся нежелательные симптомы.
Какими побочными эффектами обладает АРТ?
Побочные эффекты АРТ делят на т.н. «ранние» и «поздние»( 4). К «ранним» эффектам относят такие, как понос, тошнота, рвота, жажда, боль в животе, усталость, бессонница, выпадание волос, диспепсия. Иногда могут наблюдаться также изменения в системе кроветворения, определяемые путем простейших исследований, например, общего анализа крови (уменьшение числа нейтрофилов, или нейтропения) или биохимических исследований (повышение уровня АЛТ, АСТ ( «печеночные пробы»). Следует помнить, что все эти побочные явления могут быть кратковременными, а также то, что их возникновение ассоциируется не с АРТ в целом, а с приемом определенного препарата определенной группы (НИОТ ,ИП).
К «поздним» эффектам АРТ относят те нежелательные явления, которые могут возникать по прошествии многих месяцев или лет приема препарата. К наиболее серьезным из них относятся нарушения углеводного обмена (повышение уровня сахара в крови, вплоть до развития диабета) и изменения липидного (жирового) обмена. Эти изменения очень важно вовремя диагностировать, поскольку, в отличие от «ранних» эффектов, они могут оставаться незамеченными пациентом, и, будучи нелеченными, увеличивать риск сердечно-сосудистых заболеваний, вплоть до инфаркта.
Современная медицина располагает всеми средствами, чтобы препятствовать развитию «поздних» побочных эффектов АРТ. Самым «заметным» из них является липодистрофия, или истощение жировой ткани на фоне АРТ, ассоциирующиеся с нарушениями липидного обмена и изменениями липидного профиля пациентов(5). Данные крупных исследований показывают, что наличие липодистрофии и повышение уровня CD4+-Т-лимфоцитов у пациентов с ВИЧ имеет сильную корреляцию с увеличением риска сердечно-сосудистых событий (инфаркта)(5). Помимо этого, липодистрофия очень часто сопряжена с нарушениями липидного обмена – возрастанием уровня ХС засчет роста уровня липопротеинов низкой плотности (ЛПНП) и ТГ. Особенно часто рост уровня ХС и ТГ наблюдается у пациентов, получающих терапию ИП, усиленную ритонавиром. Поэтому одной из основных рекомендаций для пациентов, получающих ИП, является регулярный контроль показателей липидного обмена (липидограмма). За 8-12 часов до проведения этого исследования, для которого у пациента берется кровь из вены натощак, не следует есть ничего жирного, а еще лучше – не есть вообще, чтобы получить точные результаты(4). Точность результатов липидограммы у пациентов с ВИЧ приобретает первостепенное значение, поскольку нарушения липидного обмена важно диагностировать на той стадии, пока препараты АРТ не привели к выраженным нарушениям. На начальных стадиях часто эффективными оказываются изменение образа жизни и соблюдение диеты, рекомендуемой для снижения уровня ХС (антиатеросклеротическая диета), а также умеренная физическая нагрузка. Однако при неэффективности указанных мер, пациенту могут быть назначены препараты, снижающие уровень ХС и ТГ в крови – статины. Как уже упоминалось, некоторые из них вступают во взаимодействие с компонентами АРТ, поэтому назначение кардиолога следует согласовывать с лечащим инфекционистом.
Наконец, такой нежелательный поздний эффект препаратов АРТ, как рост уровня сахара в крови, легко можно купировать на начальных стадиях, пока повышенным оказывается только уровень глюкозы натощак – с помощью диеты и изменения образа жизни. Гораздо сложнее это сделать потом, когда нарушения углеводного обмена нарастают и доходит даже у развития пациента диабета 2 типа.
Именно поэтому для пациентов, получающих АРТ-терапию, первостепенное значение имеет регулярный контроль показателей углеводного (уровень сахара в крови натощак) и липидного ( уровень общего ХС и триглицеридов, а при необходимости – более расширенное исследование, т.н. липидограмма)(4). В некоторых регионах (например, на африканском континенте) такие исследования рекомендуют в качестве рутинного скрининга для всех пациентов с ВИЧ – инфекцией, как эффективное средство снижения риска ССЗ(6).
Может ли АРТ-терапия обеспечить качество жизни пациентов?
Хотя на сегодняшний день АРТ-терапия не обеспечивает полного излечения пациента, она может существенно увеличить его продолжительность жизни без ущерба для ее качества(4). Очень важно своевременно, после подтверждения диагноза, начать одну из рекомендованных ВОЗ схем терапии и тщательно ее придерживаться, сообщая лечащему врачу обо всех побочных эффектах, самочувствии на фоне терапии, дополнительно принимаемых препаратах, а также проходить назначенные обследования. Регулярное измерения уровня вирусной нагрузки иили CD4+-лимфоцитов позволяет сделать выводы об эффективности лечения, а регулярный контроль углеводного (сахар крови) и липидного ( ХС, ТГ) обмена позволит вовремя предотвратить нежелательные побочные эффекты АРТ-терапии на организм. При правильном подборе АРТ-терапии, соблюдении рекомендаций врача и регулярных контрольных обследованиях она гарантирует пациенту долгую и полноценную жизнь, ничем не уступающую жизни здорового пациента по качеству.
Источник
Ðак ÑÑÑÑÐ¾ÐµÐ½Ñ ÐÐЧ и ÐÐ ÐТ? ÐбÑÑÑнÑем на палÑÑаÑ
Мы каждый день рассказываем о вирусе иммунодефицита человека, антиретровирусной терапии, последних медицинских исследованиях и жизни людей с ВИЧ. Но при этом на русском языке практически нет доступных объяснений, как устроен сам вирус ВИЧ и как работают таблетки. Есть только зубодробительная медицинская литература и невнятные описания, из которых совершенно ничего нельзя понять. Мы исправляем этот недостаток и объясняем буквально на пальцах, как это все устроено.
Вирусы довольно трудно «убить» в обычном понимании этого слова, потому что они обладают лишь немногими признаками живого, важнейший из которых — способность размножаться. За пределами организма вирусную частицу можно разрушить с помощью агрессивных химических веществ — дезинфицирующих средств или антисептиков. Но после того как вирус проник в организм, остается только один вариант «убить» его — заблокировать размножение.
Вирусы могут размножаться только внутри клетки-хозяина, перестраивая ее работу так, что клетка начинает производить новые вирусные частицы. Это серьезно нарушает работу самой клетки и в большинстве случаев ведет к ее гибели. Процесс проникновения и размножения вируса в ней сложный и содержит много стадий, а значит, специальные лекарства могут тормозить его на различных этапах.
В случае с ВИЧ это выглядит так.
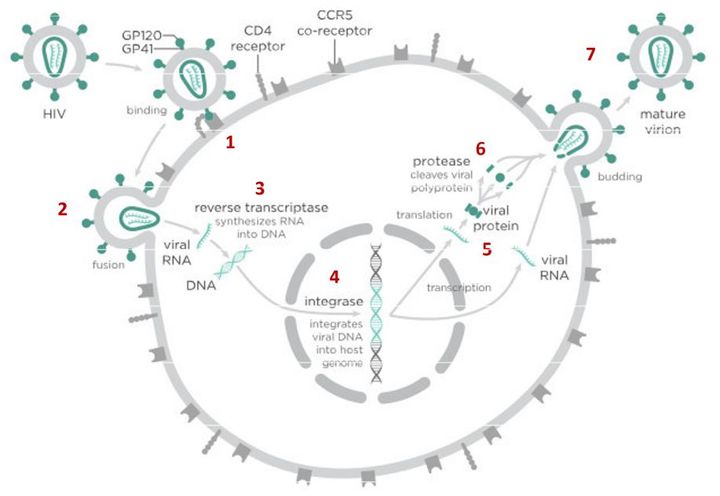
На первом этапе (цифра 1 на схеме) вирус проникает в клетку. Чтобы попасть внутрь, вирусной частице сначала необходимо «прилипнуть» к поверхности клетки. Для ВИЧ таким «клеем» является специальный белок gp120, который находится на поверхности вирусной частицы. Этот белок «приклеивается» к рецепторам CD4, расположенным на поверхности Т-лимфоцитов (Т-хелперов) и некоторых других клеток. Если у клетки нет рецептора CD4, то частица ВИЧ не может удержаться на ее поверхности и проникнуть внутрь, поэтому ВИЧ поражает только определенные типы клеток, имеющие этот рецептор. Например, некоторые Т-лимфоциты.
На этом самом первом этапе инфицирования клетки заблокировать процесс может ибализумаб — недавно зарегистрированный в США новый препарат против ВИЧ. Ибализумаб связывается с рецептором CD4 и мешает нормальному взаимодействию вирусного белка gp120 с ним. Из-за этого вирус не «прилипает» к клеткам-мишеням и не может в них проникнуть.
по теме

Лечение
Лучшие научпоп-статьи 2018 года
После «прилипания» к рецептору CD4 клетки-хозяина вирусная частица взаимодействует еще с одним рецептором — CCR5 (или с CXCR4 — в зависимости от типа вируса), чтобы лучше закрепиться на поверхности клетки. На этом этапе работает другой препарат против ВИЧ — маравирок. Молекула этого лекарства связывается с рецептором CCR5 и блокирует его, что не позволяет вирусу перейти к следующему этапу проникновения в клетку и останавливает заражение. Но у этого вещества есть недостаток — дело в том, что некоторые типы вируса иммунодефицита человека используют на втором этапе другой рецептор — CXCR4. Такому вирусу маравирок не помешает проникнуть в клетку.
После того как вирусная частица приклеилась к рецепторам CD4 и CCR5/CXCR4 и закрепилась на поверхности клетки, другой специальный белок вируса gp41 соединяет оболочку вируса с мембраной клетки-мишени и помогает вирусу проникнуть внутрь клетки (цифра 2 на схеме). На этом этапе остановить вирус может другая группа препаратов — ингибиторы слияния, например, энфувиртид. Препарат связывается с вирусным белком gp41 и нарушает его работу.
Следующий важный этап (на схеме обозначен цифрой 3) — обратная транскрипция. Для того чтобы клетка начала производить вирусные частицы, вирус должен встроить свою генетическую информацию в ДНК клетки-хозяина. Однако у ВИЧ все гены хранятся не в ДНК, как у людей, а в РНК. Поэтому вирус с помощью специального фермента — обратной транскриптазы — сначала должен переписать свои гены из собственной РНК в понятную нашим клеткам ДНК. Обратная транскриптаза работает как конвейер: захватывает отдельные нуклеозиды — строительные «кирпичики», из которых складывается ДНК, — и собирает их в готовую цепочку. А нужная (для воспроизводства вируса) последовательность кирпичиков-нуклеозидов при этом записана в исходной вирусной РНК.
На этом этапе размножение вируса блокирует очень большое количество препаратов из двух классов — нуклеозидные ингибиторы обратной транскриптазы (НИОТ — ламивудин, абакавир, тенофовир) и ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ — эфавиренз, рилпивирин). Принцип действия у веществ из обеих групп похожий: молекула лекарства связывается с обратной транскриптазой вируса, нарушает ее работу и так блокирует перенос генов вируса из РНК в ДНК. Это не позволяет генам вируса встроиться в ДНК клетки-хозяина и начать производство новых вирусных частиц.
Разница между НИОТ и ННИОТ заключается в структуре молекул лекарств. Вещества первой группы по структуре похожи на нуклеозиды — те самые кирпичики, из которых строятся молекулы ДНК и РНК. Когда такой «неправильный кирпичик» попадает в «конвейер» обратной транскриптазы вируса, ее механизм «заклинивает», и она больше не может собирать вирусную ДНК. ННИОТ имеют другую структуру, непохожую на нормальные нуклеозиды, и блокируют обратную транскриптазу, связываясь с ее молекулой в других точках.
С этой особенностью строения связано и большее число побочных эффектов при приеме НИОТ по сравнению с ННИОТ: молекулы первого класса ингибиторов могут нарушать процессы синтеза РНК и ДНК и в наших собственных клетках, так как они похожи на «нормальные» нуклеозиды и тоже «заклинивают» наши собственные ферменты, но в гораздо меньшей степени, чем вирусные. НИОТ исторически были первым классом препаратов, которые начали использовать для лечения ВИЧ-инфекции.
На следующем этапе инфицирования (цифра 4 на схеме) готовая вирусная ДНК проникает в ядро и встраивается в ДНК клетки-хозяина с помощью специального вирусного фермента — интегразы. Работу этого фермента блокируют ингибиторы интегразы, например, долутегравир, не позволяя ДНК вируса встроиться в наши гены.
После того как вирусная ДНК встраивается в ДНК клетки-хозяина, клетка получает неправильную программу и начинает производить вирусные белки и РНК, необходимые для сборки новых частиц вируса (цифра 5 на схеме), используя для этого структуры, которые в норме производят собственные белки клетки. Такая перенастройка производства белка сильно нарушает работу клетки и через некоторое время вызывает ее гибель. Лекарств, которые бы влияли на этот этап размножения вируса, нет, так как здесь вирус использует собственные ферментные системы клетки-хозяина и блокирование их работы какими-то веществами навредит здоровым клеткам.
по теме

Лечение
Ошибка системы. Почему в регионах опять не хватает таблеток от ВИЧ
После синтеза вирусных белков клеткой-хозяином в работу вступает еще один фермент вируса — протеаза (цифра 6 на схеме). Дело в том, что белки ВИЧ синтезируются в виде длинных цепочек белков-предшественников, но они неактивные. Протеаза разрезает эти цепочки на более короткие фрагменты, которые становятся активными белками вируса: из одних собирается вирусная оболочка, другие выполняют функции ферментов (обратная транскриптаза, интеграза, протеаза, о которых мы говорили выше). Класс лекарств, нарушающих работу вирусной протеазы, включает большое количество препаратов от достаточно старого лопинавира до современного дарунавира. Основной недостаток препаратов этого класса — высокая степень перекрестной устойчивости: если вирус приобретает устойчивость к одному препарату, скорее всего, на него не подействует ни один другой препарат из этого класса.
На последнем этапе (цифра 7 на схеме) вирусные частицы собираются из готовых компонентов (синтезированных клеткой вирусных белков и РНК), как конструктор, и покидают клетку-хозяина. Лекарств, которые бы тормозили эти процессы, пока не существует.
ВИЧ имеет высокую склонность к мутациям, что позволяет ему быстро приобретать устойчивость к лекарствам. Мутации изменяют форму молекул ферментов вируса. Если при этом форма изменится существенно, то фермент не сможет нормально работать и такой вирус размножаться перестанет — это вредная для вируса мутация. Однако в некоторых случаях — при полезных мутациях — форма молекулы фермента меняется не сильно, а так, что сам фермент продолжает нормально работать, но молекула лекарства уже не может с ним связаться.
Поэтому для эффективного подавления размножения ВИЧ обычно назначают три разных препарата из разных групп, влияющих на разные ферменты вируса, блокируя его воспроизводство на разных этапах. Исключением является группа ингибиторов обратной транскриптазы (НИОТ и ННИОТ) — эти лекарства связываются с разными участками молекулы вирусного фермента, поэтому могут назначаться вместе, несмотря на то, что относятся к одной группе. В условиях такой терапии вирусу очень трудно выработать устойчивость, потому что одновременно должно произойти несколько полезных мутаций в разных генах вируса, а это бывает крайне редко.
Мутации помогают не только ВИЧ, но и некоторым людям. Например, мутация, изменяющая форму рецептора CCR5, который ВИЧ использует на первом этапе проникновения в клетку, делает человека полностью невосприимчивым к некоторым подтипам ВИЧ. Вирус не может «приклеиться» к такому рецептору и проникнуть в клетку. В разных популяциях людей распространенность этой мутации колеблется от 0,1 % до 1 %.
Несмотря на большое количество разных групп препаратов, используемых для торможения ВИЧ-инфекции, вылечить ее полностью пока невозможно. Проблема заключается в том, что все имеющиеся на сегодняшний день лекарства тормозят размножение вирусов в организме на разных этапах, но неспособны полностью удалить вирус из организма. Он всегда будет присутствовать в каком-то количестве клеток в «спящем режиме», встроившись в ДНК, и сразу же продолжит размножение, как только человек прекратит прием антиретровирусных препаратов.
Есть несколько перспективных технологий, например, CRISPR/Cas9, которые могут позволить полностью удалить вирусную ДНК из организма человека, но пока ни одна из них не прошла все необходимые исследования для подтверждения эффективности и безопасности. Исследования продолжаются.
Источник