Экспериментальная группа по вич
Содержание статьи
Эксперимент с генами на себе: как ВИЧ-активист Мэтт Шарп внес вклад в науку

Вот уже десяток лет группа ВИЧ-активистов помогает разрабатывать генную терапию, в том числе и участвуя в экспериментах. СПИД.ЦЕНТР публикует перевод статьи The Atlantic.
Мэтт Шарп спокойно наблюдал, как медсестра закрепила иглу капельницы в его руке. Шарп знал, на что идет: будучи одним из первых людей, на которых испытывали экспериментальный метод лечения, он мог в итоге получить дозу бешеных клеток-мутантов. Но он был так заворожен целью эксперимента, что не волновался. За те двадцать лет, что Шарп жил с ВИЧ, он успел увидеть, как на пике эпидемии СПИДа болезнь унесла жизни дюжин его друзей и возлюбленных. Он был убежден, что в этот день делает шаг к исцелению.
Несколькими месяцами ранее ученые взяли белые кровяные тельца Шарпа и с помощью крохотных молекул изменили их ДНК, удалив один ген в каждой клетке. Теперь ему предстояло переливание крови, которое вернет измененные клетки в его кровяной поток. Задача этой процедуры заключалась в том, чтобы изменить генетическую структуру клеток и сделать тело Шарпа устойчивым к ВИЧ. Такого рода лечение уже применялось при других заболеваниях, но эксперименты поставили на паузу после смерти молодого человека в 1999 году. Тело Шарпа позволит исследователям проверить безопасность нового молекулярного инструмента под названием «цинковые пальцы».
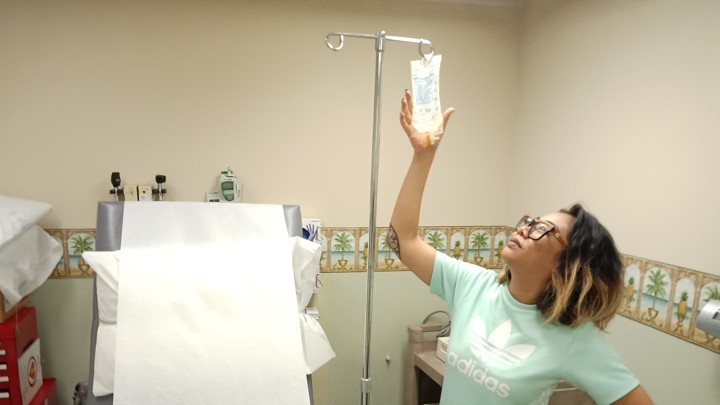 Грейс Гонзага из Центра клинических исследовний Quest в комнате, где она вливала отредактированные гены Мэтту Шарпу.
Грейс Гонзага из Центра клинических исследовний Quest в комнате, где она вливала отредактированные гены Мэтту Шарпу.
Переливание крови было проведено в июне 2010 года в Центре клинических исследований Quest, неприметном сером здании неподалеку от квартала Филмор в Сан-Франциско. Замороженные клетки Шарпа доставили в заполненном жидким азотом контейнере, похожем на робота R2-D2 из «Звездных войн». Разморозив их в емкости с горячей водой, медсестра подсоединила пакет к его капельнице. Мутная желтая жидкость медленно втекала в руку Шарпа. Спустя 30 минут он поехал на работу, пока миллиарды генетически измененных клеток делились в его артериях и венах.
В последнее десятилетие пациенты с ВИЧ, такие как Шарп, оказались в авангарде научных исследований редактирования генов. Благодаря тому, что сообщество людей с ВИЧ имеет активную правозащитную сеть, а гены, из-за которых люди инфицируются ВИЧ, хорошо известны, пациенты с этим заболеванием становятся идеальными добровольцами инновационных — пусть иногда и рискованных — экспериментов. Методика редактирования генов, связанных с ВИЧ, потрясла медицинское и научное сообщество в прошлом месяце, когда китайский исследователь Хэ Цзянькуй сделал шокирующее заявление, что он изменил геномы не инфицированных ВИЧ детей-близнецов, дабы сделать их устойчивыми к инфекции. Этот безрассудный секретный эксперимент был широко осужден научными кругами. Однако взрослые пациенты с ВИЧ добровольно участвуют в экспериментах, на которые наука закрывает глаза, прокладывая дорогу для будущей работы над генетической терапией, например, рака и слепоты.
Китайского ученого, создавшего генетически модифицированных детей, могут казнить. Он обвиняется в коррупции и взяточничестве, за которые в Поднебесной полагается смертная казнь. Как сообщает The Telegraph, сейчас китайский ученый Хэ Цзянькуй находится под домашним арестом в городе Шэньчжэнь, где расположен университет, в котором ранее работал генетик. По информации издания, с помощью взяток исследователь пытался продвигать свои научные изыскания. Так, Цзянькуй заработал около $50 тыс, продавая технологии секвенирования генома, которые в итоге и мог пустить на финансирование своих исследований.
То, что произошло с Шарпом, после того как он подписался на революционное переливание крови, демонстрирует, как редактирование ДНК потенциально может расширить человеческие возможности и что генетическая медицина в качестве панацеи имеет свои пределы.
Шарп, которому сейчас 62, продвигал инновационную экспериментальную медицину с 1980 годов. По его словам, как ветерана активистской организации СПИД-коалиция для мобилизации силы (ACT UP) его арестовывали как минимум 8 или 9 раз — он не помнит точно — во время выступлений против замедленного изучения и поиска способов лечения ВИЧ. Впервые он встретил основателя центра Quest Джея Лалезари в Сан-Франциско в начале 90-х, когда молодой доктор еще только делал себе имя дерзкими экспериментами с потенциально токсичными препаратами. Исследования Лалезари давали людям с ВИЧ надежду на жизнь, но с активистами у него сперва сложились непростые отношения: ACT UP устроила радикальную акцию протеста на одном из его выступлений на конференции по ВИЧ.
Со временем активисты начали доверять Лалезари. Сегодня сотни людей благодарны ему за спасение их жизней. В 2008 году Лалезари участвовал в исследовании генной терапии, которое спонсировала компания Johnson&Johnson. Результаты получились невпечатляющими. Так что, когда маленькая биотехнологическая компания Sangamo Therapeutics предложила ему провести исследование редактирования генов с помощью новой технологии «цинковые пальцы», он скептически отнесся к перспективам этой методики. Однако тщательно изучив ее, он решил провести эксперимент и подписал на него 65 пациентов с ВИЧ.

Когда Шарп узнал об исследовании генного редактирования, он схватился за возможность поучаствовать и согласился стать пациентом номер 2 в проверке безопасности метода. Ко всеобщему облегчению после переливания крови Шарп столкнулся только с одним побочным эффектом: его тело стало издавать сильный запах. Когда на следующий день он вернулся в Quest для анализов, медсестра узнала о его появлении, стоило ему войти в дверь. Документация Sangamo подтверждает, что химическое вещество, которое они используют, может привести к появлению чесночного запаха, который пройдет в течение нескольких дней. Однако медсестры говорят, что Шарп и его коллеги по эксперименту скорее начали пахнуть, как протухшая кукурузная каша.
по теме

Лечение
Лиссабонский пациент: человеку с ВИЧ скоро исполнится 100 лет
Когда стали известны результаты анализов, Шарп обнаружил, что его показания в медкарте улучшились потрясающим образом. Впервые с тех пор, как ему поставили диагноз ВИЧ, количество его иммунных клеток — ключевой маркер работы иммунной системы — подскочило до нормального, здорового уровня. Шарп хотел присутствовать среди зрителей на ведущей конференции по ВИЧ, когда эти данные станут доступны, так что в феврале 2011 года он полетел в Бостон. Он еще не знал, не был ли его результат случайным колебанием. Когда Лалезари вывел на экран слайд, демонстрирующий значительное повышение числа иммунных клеток других пациентов, по словам Шарпа, в зале все ахнули.
Процедуры, которые пришлось перенести Шарпу в следующие несколько лет, были более неприятными, чем первое переливание крови. Во время ректальной биопсии он смотрел на экран, который показывал «как игла вошла в мой зад, куда она двинулась и откуда конкретно они взяли пробу», — рассказывает Шарп. Он был под местным обезболивающим и не чувствовал боли, так что комментировал процедуру низким зловещим голосом: «Приступаем к путешествию в центр Земли».
Ректальная биопсия, анализы крови и другие анализы не выявили никаких серьезных осложнений у участников исследования. Но ситуация Шарпа была нетипичной. Другие пациенты все-таки столкнулись с заметными побочными эффектами, включавшими жар, озноб, головную и мышечную боль. Одно исследование утверждает, что это скорее реакция организма на вливание миллиардов клеток, чем на их генетические изменения. Но были и другие проблемы. Трехлетнего периода, во время которого ученые наблюдали за здоровьем пациентов, могло не хватить, чтобы выявить осложнения, способные проявиться в долгосрочной перспективе, например, рак, вызванный повреждением генов в ходе эксперимента.
 Мэтт Шарп
Мэтт Шарп
Что самое важное — эксперимент не осуществил мечту о полном исцелении. Некоторые пациенты не демонстрировали заметного улучшения. В случае Шарпа улучшение иммунной системы было стойким. Он пришел к выводу, что участие в исследовании того стоило, но он все равно каждый день принимает свои лекарства, чтобы держать вирус под контролем. Другие пациенты утверждают, что они «исцелились» и прекратили принимать стандартные лекарства, потому что их тела фактически стали способны контролировать ВИЧ.
Лалезари говорит, что бросаться словом «исцеление», обсуждая эксперимент, — безответственно. Его итог был впечатляющим, но предварительным: «Главным результатом была безопасность», — говорят исследователи. Однако современные лекарства от ВИЧ более безопасны, могут сократить присутствие инфекции до неопределяемого уровня и становятся все более доступными. Лалезари отмечает, что есть другие экспериментальные способы лечения ВИЧ, например, с помощью антител, медицинских препаратов, низкомолекулярных средств, которые выглядят более многообещающими, чем редактирование гена.
Самым важным следующим шагом для Лалезари после его выступления в 2011 году в Бостоне было продолжить исследования. Если бы он смог добиться полного исцеления, о котором говорят некоторые из его пациентов, редактирование гена и правда перевернуло бы сферу борьбы с ВИЧ. Но его работа внезапно встала, столкнувшись с суровой реальностью инновационной науки — проблемами с финансированием. Sangamo Therapeutics, биотехнологическая компания, которая оплатила первое исследование, решила сократить ВИЧ-направление и вместо этого с помощью своей технологии редактирования генома стала разрабатывать лекарства от других болезней.
по теме

Лечение
Жизнь без таблеток: как я получаю инъекционную терапию
Это разъярило ВИЧ-активистов. «Компания отправила проект в долгий ящик, потому что они не смогли придумать, как им заработать денег», — говорит Марк Харрингтон, исполнительный директор Treatment Action Group в Нью-Йорке. Шарп, разочарованный задержкой, подписал открытое письмо к Sangamo, призывая компанию к новым инициативам по исследованиям. «Они просто отказались продолжать изначальный эксперимент и оплатить дальнейшие исследования», — говорит он.
Причины, по которым финансирование прекратилось, неоднозначны. В 2013 году Sangamo купалась в деньгах после подписания сделки на 320 000 000 долларов. Но потом их акции упали из-за инсайдерского биржевого скандала, погрузившего компанию в хаос. Комиссия США по ценным бумагам и биржам обвинила тогдашнего вице-президента отделения медицинских исследований Sangamo Уинсона Танга в возможном участии в мошеннической схеме, которая принесла компании более полутора миллионов долларов «нелегальных доходов».
«Когда Уинсон Танг отправился в тюрьму, Sangamo совершенно забросила проект, — рассказывает Лалезари, который поддерживает контакты с биотехнологической компанией на случай, если им еще удастся провести исследования. — Если вы собираетесь работать с бизнесом, помните, что вы танцуете с дьяволом».
Сэнди Макри, президент и CEO Sangamo, оспаривает этот вывод, утверждая, что решение отложить тему ВИЧ возникло до биржевого скандала Уинсона Танга. Однако компания признает, что они не считают исследование ВИЧ особо ценной инвестицией. Макри возглавил Sangamo в прошлом году, вскоре после того, как акции компании упали примерно до 3 долларов за акцию, и с тех пор старался восстановить ее позиции. Центральный офис компании приютился в Ричмонде (Калифорния), городе на краю залива Сан-Франциско, между магазином лодочных запчастей, железнодорожным депо, нефтеперерабатывающим заводом Shevron, яхт-клубом и Национальным парком имени Рози Клепальщицы.
«Мне пришлось принять решение, на что потратить наш портфель акций, — говорит Макри, отмечая, что существующие лекарства от ВИЧ и так эффективны. — Мы могли выбрать только несколько из направлений. Я посмотрел на опыты с ВИЧ. Там сделали немало, пытаясь создать новый продукт. Но текущая версия… далека от завершения».

Однако Шарп непоколебим. Не сумев выбить средства из Sangamo, он начал лоббировать проект среди госчиновников США и исследователей ВИЧ. Отчасти благодаря его усилиям Рафик-Пьер Секали, профессор медицинского факультета университета Кейс Вестерн Резерв, вдохновился продолжать исследование редактирования генов в терапии ВИЧ. В этом году Национальный институт здравоохранения выделил Секали 11 000 000 долларов на новый эксперимент под названием Trailblazer, и ему удалось оплатить использование технологии, принадлежащей Sangamo.
Шарп «всегда был крайне страстным человеком. Он всегда был очень настойчивым, подталкивал нас к большему», — отмечает Секали. Теперь новый отряд пациентов с ВИЧ присоединяется к эксперименту Секали. Они помогают создать будущее, в котором редактирование гена может стать рутинной частью медицинского ухода.
Каким именно окажется это будущее, нам еще предстоит увидеть. «Если бы нас всех можно было перестроить, чтобы мы стали устойчивы к ВИЧ, то стигма, окружающая болезнь, полностью бы исчезла», — говорит Шарп. Если технологии станут более эффективны, будет возможно избавиться от целого ряда генетических заболеваний. Но редактирование гена влечет за собой определенные риски, не считая просто технических сложностей. Существующая генная терапия очень дорога, доходит до 475 000 долларов за процедуру. Редактирование гена может привести к новой эре неравенства в медицине, не говоря уже о том, что людей пугает идея «детей на заказ» или опыты на младенцах с целью сделать их устойчивыми к ВИЧ с рождения.
Есть и более неожиданные и непредсказуемые перспективы. Квир-теоретик Тим Дин, известный нестандартным взглядом на традиционные сценарии, рассуждает о том, что редактирование гена может создать новое классовое расслоение в культуре знакомств гомосексуальных мужчин. «Я предвижу некое технологически продвинутое будущее, в котором на сайтах знакомств появляется отметка, показывающая, был ли ваш ген отредактирован или нет», — рассуждает он.
Шарп же просто хочет, чтобы исследование нового средства двигалось вперед. Ему не важно, будет это редактирование ДНК, антитела или новые таблетки. «Я уже участвовал в 12 медицинских экспериментах, — объясняет он. — И я готов попробовать что угодно, если мне покажется, что это может сработать».
Источник
Почему в XXI веке стоит перестать бояться диагноза ВИЧ
С тех пор, как в 1983 году ученые открыли вирус иммунодефицита человека, прошло почти 40 лет. Сегодня диагноз «ВИЧ-инфекция» не приговор, а благодаря открытию высокоактивной антиретровирусной терапии само заболевание перешло в разряд контролируемых.
Однако страхи и предрассудки, связанные с ВИЧ и его терминальной стадией — СПИДом, живы и сейчас. Причина — в нехватке знаний. Именно это приводит к тому, что люди, получившие положительный тест, воспринимают диагноз трагически, а общество стигматизирует ВИЧ-инфицированных. В материале ТАСС — об истории возникновения вируса, поиске лекарств и опасных мифах.
История одного вируса
О страшном вирусе, пришедшем от обезьян, активно заговорили в 80-е годы прошлого века. Предполагается, что он появился в Конго еще в 60-х, а потом перекинулся с африканского континента в Америку и пошел по свету. В начале 80-х, когда стало известно о первых заболевших, никто не понимал, что происходит с людьми и как их лечить.
В 1981 году вышла первая научная статья, описывающая СПИД, а в 1983-м ученые из двух стран — из Института Пастера во Франции и Национального института рака в США — независимо друг от друга открыли вирус иммунодефицита человека, вызывающий синдром приобретенного иммунодефицита (СПИД). Уже в 1985 году появился первый лицензированный тест на ВИЧ. Советские люди узнали о СПИДе одними из последних: первый случай заболевания зарегистрирован в СССР в 1986 году.
Вирус стремительно распространялся по планете: уже к 1991 году его диагностировали у десяти миллионов, а к началу XXI века СПИД унес жизни 21,8 миллиона человек.
Ученые установили, что ВИЧ — ретровирус, который поражает клетки иммунной системы и делает организм уязвимым для внешних агентов, атакующих иммунитет. Иммунодефицит, развивающийся в результате заражения ВИЧ-инфекцией, приводит к повышенному риску возникновения у человека ряда заболеваний, которым здоровая иммунная система может противостоять. ВИЧ-инфицированные заболевают туберкулезом в сто раз чаще здоровых людей. Кроме того, у них чаще развиваются онкология и оппортунистические инфекции — заболевания, вызванные условно-патогенными вирусами, бактериями или простейшими. К таким, например, относятся герпес, кандидоз и вирус папилломы человека.
На протяжении многих лет информация о смертельной опасности заболевания вызывала панику и порождала мифы. В то же время очевидная опасность болезни заставила ученых всего мира сплотиться и начать поиски эффективной терапии.
Сегодня, когда с ВИЧ-инфекцией в мире живет более 38 миллионов человек, такая терапия существует и доступна во многих странах. Речь об антиретровирусной терапии (АРВТ). И, хотя препарат для полного излечения от вируса еще не изобрели, благодаря современным лекарствам заболевание перешло в разряд полностью контролируемых. ВИЧ-положительный человек, принимая назначенные врачом препараты, живет обычной жизнью.
Путь к одной таблетке
Путь к созданию эффективных лекарств был нелегким. Поначалу, как и в случае с пандемией COVID-19, ученые пытались использовать те лекарственные средства, которые уже существовали на рынке. Тогда надежды возлагали на противораковый препарат, но они не оправдались.
Эра антиретровирусной терапии началась с регистрации в 1987 году нового препарата. Он многие годы входил в клинические рекомендации по лечению пациентов, но со временем выяснилось, что вирус способен спонтанно мутировать в организме и быстро обретать к препарату устойчивость.
Поиски действенной терапии продолжились. В начале 1990-х пришло понимание, что одной таблетки для лечения этого заболевания недостаточно: ученые стали разрабатывать комбинации различных препаратов. Появились новые лекарства из группы нуклеозидных ингибиторов обратной транскриптазы (НИОТ). Эти антиретровирусные препараты структурно схожи с органическими соединениями, входящими в состав рибонуклеиновой кислоты (РНК) и дезоксирибонуклеиновой кислоты (ДНК) — они могут конкурентно блокировать определенный фермент ВИЧ и замедлять синтез вирусной ДНК.
Дело в том, что все гены у этого вируса хранятся в РНК, а у людей — в ДНК. Поэтому для размножения вирус с помощью обратной транскриптазы должен переписать свои гены из одного формата в другой. Препараты из группы НИОТ мешают этому процессу: не дают вирусу переносить гены из РНК в ДНК.
Однако в 1993 году на международной конференции по СПИДу ученые огласили данные исследования, согласно которому, сочетание лекарств только этой группы не дает долгосрочного эффекта. Примерно в это же время начали использовать новую группу препаратов — ингибиторы протеазы, действующие на другой фермент вируса. А в 1996 году появился еще один класс антиретровирусных препаратов — ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ). Как и НИОТы, препараты этого класса блокируют фермент вируса, мешая построению РНК ВИЧ, то есть размножению вируса.
Ученые выяснили, что сочетание лекарств из нескольких групп препаратов прекращает размножение вируса в организме, поскольку препараты влияют на разные ферменты вируса, блокируя его воспроизведение на разных этапах.
Это открытие легло в основу новой трехкомпонентной терапии ВИЧ-инфекции, разработанной в 1996 году. Она и сейчас остается основой большинства известных схем АРВТ. В нее входит два препарата НИОТ и третий, отличающийся по своему действию.
С 1997 года ВИЧ стал контролируемой хронической инфекцией, а люди, которые получают лекарства, перестают умирать от СПИДа. Вирусная нагрузка у людей, принимающих антиретровирусную терапию, снижена до неопределяемого уровня, они могут создавать семьи с ВИЧ-отрицательными партнерами, рожать здоровых детей, что было невозможно представить себе еще в 80-е годы. И теперь в лечении таких пациентов появилась новая цель: предоставить людям, живущим с ВИЧ, максимально удобные препараты, которые не будут влиять на их жизнь, позволят свести риск развития резистентности (невосприимчивости к терапии) и появления побочных эффектов к минимуму.
С каждым годом появляется все больше новых препаратов и даже новых групп препаратов, токсичность терапии постоянно снижается. Так, в 2007 году появился еще один новый класс препаратов — ингибиторы интегразы, которые блокируют внедрение ВИЧ в ДНК клетки хозяина. В настоящее время этот класс насчитывает пять различных препаратов.
Другим большим достижением фармацевтики стала разработка препаратов по типу «два или три в одном», в которых сочетаются лекарства разных групп. В 2006 году на рынок вышел первый комбинированный препарат, который содержит трехкомпонентную схему в одной таблетке. Сегодня таких комбинированных препаратов на рынке около 30.
Эти лекарства эффективны по нескольким причинам. Прежде всего, такая схема намного удобнее: человек пьет всего одну таблетку в день и может выбирать комфортное для себя время приема, не нужно подстраивать весь день под график терапии. Кроме того, риск забыть выпить одну таблетку намного ниже, а процент пациентов, которые придерживаются лечения, выше. Когда человек принимает несколько таблеток несколько раз в день, всегда есть шанс случайно не выпить один из препаратов в схеме или пропустить полностью прием терапии, а это повышает риск развития невосприимчивости к лекарствам.
Еще один важный момент: период полувыведения препарата из организма в случае со схемами «одна таблетка один раз в день» длиннее, поэтому даже если человек по каким-то причинам не сможет принять препарат, то на следующий день у него будет достаточная концентрация активных веществ лекарства в организме для поддержания приверженности. И, конечно, большинство новых препаратов вызывают меньше побочных эффектов.
К 2014 году масштабное применение АРВТ помогло предотвратить около 7,8 миллиона смертей. Меняется и тактика лечения: если поначалу врачи назначали терапию пациентам с высокой вирусной нагрузкой, то теперь, согласно новым клиническим рекомендациям ВОЗ, лечение должны получать все в кратчайшие сроки после постановки диагноза «ВИЧ-инфекция».
На современном этапе перед медициной стоят новые задачи: добиться полного освобождения от вируса. Кроме того, мировое медицинское сообщество ждет появления первых препаратов инъекционной терапии пролонгированного действия. Их разработка началась в 2010-х. Они позволят заменить ежедневный прием таблеток инъекционным введением лекарства раз в два месяца, что еще больше упростит лечение.
Современная АРВТ состоит из одного комбинированного препарата или нескольких монопрепаратов. В России чаще назначают многокомпонентную терапию. Комбинированные препараты получают в основном дети, а также пациенты, у которых возникают сложности с приемом терапии или резистентность к схемам, состоящим из монопрепаратов.
Правда или ложь
Столкнувшись с диагнозом впервые, люди ищут информацию в Интернете и находят непроверенные и устаревшие данные, а иногда и откровенную ложь. Движение ВИЧ-диссидентов распространяет информацию о бесполезности лечения: по их мнению, терапия приводит к проблемам со здоровьем и даже летальным исходам.
Проблема в том, что доступной информации о высокоактивной антиретровирусной терапии не так много или написана она сложным наукообразным языком. В результате люди до сих пор верят мифам, связанным с ВИЧ и АРВТ. При ближайшем рассмотрении эти мифы легко развенчать.
1. ВИЧ-положительные люди не могут иметь отношений с ВИЧ-отрицательными людьми, потому что могут инфицировать близких.
Иногда люди боятся подойти к ВИЧ-инфицированному, обнять его. На самом деле ВИЧ не распространяется воздушно-капельным путем и через общие предметы быта. Вирус иммунодефицита человека передается исключительно через кровь, сперму, материнское грудное молоко и другие биологические жидкости. Столкнувшись с кислородом, вирус погибает.
При этом, если ВИЧ-инфицированный принимает назначенные лекарства правильно, при достижении неопределяемой вирусной нагрузки он не заразит партнера даже при незащищенном сексе. Иногда достичь полной неопределяемости вируса можно за две недели терапии, однако считается, что человек не передает ВИЧ только спустя полгода после первого анализа с неопределяемой нагрузкой. Однако даже в этом случае не стоит отказываться от средств барьерной контрацепции: они защищают от многих других заболеваний.
2. ВИЧ-положительным нельзя иметь детей.
Сегодня многие пары с положительным статусом ВИЧ имеют здоровых детей. По статистике, если ВИЧ-положительная женщина соблюдает рекомендации врачей во время беременности, шансы родить здорового младенца составляют 98-99%. При отсутствии же противовирусной профилактики у беременной во время родов и в течение первого времени жизни ребенка ВИЧ передается в 20-40% случаев. Если у беременной впервые выявляют ВИЧ, ей сразу же назначают антиретровирусные препараты для профилактики перинатальной передачи вируса: женщине — в периоды беременности и родов, ребенку — в течение первых четырех недель жизни. Кроме того, новорожденного переводят на искусственное вскармливание сразу после рождения, чтобы минимизировать риск заражения.
3. От ВИЧ умирают.
Сегодня мировая медицина считает ВИЧ хронической инфекцией, поддающейся контролю. Опыт показал, что, если принимать современные препараты, ВИЧ-положительные люди живут столько же, сколько в среднем обычный человек.
Люди с ВИЧ-инфекцией могут принимать антиретровирусные препараты и вести нормальный образ жизни, пока ученые придумывают лекарство, способное раз и навсегда остановить вирус.
4. ВИЧ распространен только внутри традиционных групп риска.
Последний, но самый важных миф. ВИЧ вышел за пределы традиционных групп риска — людей, употребляющих инъекционные наркотики, представителей ЛГБТ-сообщества и секс-работниц. Более 60% новых случаев инфицирования связаны с гетеросексуальными контактами. Поэтому каждый человек должен ответственно относиться к своему здоровью и здоровью близких: использовать барьерные средства контрацепции и регулярно, раз в полгода-год, сдавать анализ на ВИЧ. Часто передача вируса происходит именно из-за незнания своего статуса и несвоевременного начала приема антиретровирусных препаратов.
Источник