Микобактериальная инфекция при вич
Содержание статьи
Болезнь, вызванная ВИЧ, с проявлениями микобактериальной инфекции
Рубрика МКБ-10: B20.0
МКБ-10 / A00-В99 КЛАСС I Некоторые инфекционные и паразитарные болезни / B20-B24 Болезнь, вызванная вирусом иммунодефицита человека ВИЧ / B20 Болезнь, вызванная вирусом иммунодефицита человека ВИЧ, проявляющаяся в виде инфекционных и паразитарных болезней
Определение и общие сведения ( в т.ч. эпидемиология)[править]
Mycobacterium Avium Complex (МАС-инфекция)
Частое осложнение СПИДа — диссеминированная инфекция, вызванная Mycobacterium avium-intracellulare (Mycobacterium avium complex). Показано, что эта инфекция значительно снижает продолжительность жизни больных СПИДом, а ее лечение приводит к улучшению состояния и повышает выживаемость. Риск инфекции, вызванной Mycobacterium avium-intracellulare, особенно высок при значительном снижении числа лимфоцитов CD4. Это инфекционное осложнение возникает в течение года примерно у 8% больных, число лимфоцитов CD4 у которых ниже 100 мкл-1. Если число лимфоцитов CD4 более 100 мкл-1, диссеминированная инфекция, вызванная этим возбудителем, возникает гораздо реже.
Этиология и патогенез[править]
Mycobacterium avium-intracellulare — условно-патогенные микроорганизмы, которые обычно обнаруживаются в почве и воде. Наиболее частый источник заражения — загрязненная вода.
Клинические проявления[править]
Как правило, диссеминированная диссеминированная инфекция, вызванная Mycobacterium avium-intracellulare (Mycobacterium avium complex) не имеет специфической клинической симптоматики. Большинство пациентов предъявляют жалобы на высокую лихорадку (более 40 °С), выраженную потерю массы тела (более 10% массы тела), диарею, боли в животе. При наличии подобной симптоматики у больного с ВИЧинфекцией с количеством CD4-лимфоцитов менее 100 клеток/мкл необходимо исключить микобактериоз. Возможно развитие очаговых поражений в виде лимфаденитов различной локализации (шейные, паховые, брюшные лимфатические узлы), остеомиелита (позвонков), артритов, поражений кожи. При ультразвуковом исследовании часто регистрируют увеличение размеров печени и селезенки.
Болезнь, вызванная ВИЧ, с проявлениями микобактериальной инфекции: Диагностика[править]
Подтвердить диагноз микобактериоза можно на основании выделения Mycobacterium avium-intracellulare при посеве крови, пунктата костного мозга, биопсийного материала. Обнаружение микобактерий в кале, мокроте или бронхоальвеолярном лаваже при отсутствии клинической симптоматики может свидетельствовать только о колонизации слизистых. Терапию в таких случаях назначать нецелесообразно.
Дифференциальный диагноз[править]
Болезнь, вызванная ВИЧ, с проявлениями микобактериальной инфекции: Лечение[править]
Пациентам показано назначение комплексной терапии, включающей макролиды (кларитромицин по 500 мг 2 раза в сутки или азитромицин по 600 мг 1 раз в сутки) в сочетании с этамбутолом (1200 мг/сут) и рифабутином (300 мг/сут). Продолжительность терапии, как правило, составляет не менее 6 мес.
При одновременном использовании АРВТ лечение микобактериоза можно прекратить после повышения количества CD4-лимфоцитов (более 100 клеток/мкл). Доза кларитромицина обычно не превышает 500 мг 2 раза в сутки. Вместо кларитромицина можно назначать азитромицин, который меньше влияет на систему цитохрома P-450. В качестве резервных препаратов применяют: амикацин (15 мг/кг в сутки внутривенно), фторхинолоны (левофлоксацин по 500 мг внутрь 1 раз в сутки, ципрофлоксацин по 500-750 мг внутрь 2 раза в сутки).
Существуют лекарственные взаимодействия кларитромицина и ряда АРВП: AUC (площадь под кривой) кларитромицина повышается при одновременном приеме с индинавиром (на 50%), ритонавиром (на 75%), ампренавиром (на 18%), лопинавиром/ритонавиром (на 77%), атазанавиром (на 94%), невирапином (на 26%) и саквинавиром (на 177%). При совместном приеме атазанавира и кларитромицина последний следует использовать в половинной дозе или назначить другой препарат, поскольку повышение концентрации кларитромицина увеличивает риск удлинения интервала Q-T на кардиограмме.
Одновременный прием кларитромицина и указанных выше АРВП не требует коррекции дозы кларитромицина, за исключением сочетания кларитромицина с лопинавиром/ритонавиром или ритонавиром у больных с почечной недостаточностью. Одновременный прием эфавиренза снижает концентрацию кларитромицина на 39%, поэтому целесообразно заменить его азитромицином.
Профилактика[править]
Больным с ВИЧ-инфекцией при количестве CD4-лимфоцитов менее 50 клеток/мкл можно назначить профилактику микобактериозов макролидами (азитромицин по 1200 мг 1 раз в неделю) или рифабутином (ежедневно по 150 мг). При увеличении числа CD4-лимфоцитов более 100 клеток/мкл можно прекратить первичную профилактику (через 3 мес) и поддерживающую терапию (через 6 мес).
Прочее[править]
Развитие МАС-инфекции как проявление синдрома восстановления иммунитета
Клиническая симптоматика микобактериоза обычно развивается в течение первых 3 мес после начала АРВТ (в раде случаев синдром восстановления иммунитета наблюдают через 6-8 мес) у больных с исходно низким количеством CD4-лимфоцитов (менее 50 клеток/мкл) и хорошим вирусологическим и иммунологическим ответом на лечение (РНК ВИЧ <50 копий/мл; CD4-лимфоциты >100 клеток/мкл). Как правило, клинические проявления МАС-инфекции включают лихорадку, увеличение лимфатических узлов шеи, средостения, брыжейки. Возможно развитие перикардита, остеомиелита, кожных абсцессов, бурситов, поражения ЦНС.
Терапевтическая тактика включает: продолжение АРВТ по прежней схеме, терапию МАС-инфекции, применение нестероидных противовоспалительных средств и в ряде случаев стероидов (преднизолон — по 20-40 мг/сут в течение 4-8 нед).
Источники (ссылки)[править]
ВИЧ-инфекция и СПИД [Электронный ресурс] : национальное руководство / под ред. акад. РАМН В.В. Покровского. — М. : ГЭОТАР-Медиа, 2013.
Дополнительная литература (рекомендуемая)[править]
Действующие вещества[править]
- Амикацин липосомальный
Источник
Атипичные микобактериозы у ВИЧ-инфицированных
Этиология.
Разнообразие атипичных микобактерий представлено в таблице 14. Выделяют 4 группы Ryuniona (I, II, III, IV). Говоря об атипичных микобактериях, обычно подразумевают Mycobacterium avium-intracellulare (другое название — Mycobacterium avium complex, MAC), так как по частоте вызываемых инфекций этот вид далеко опережает все другие, включая M.celatum, M.kansasii, M. xenopi и M.geense.
Эпидемиология.
Бактерии MAC распространены повсеместно, они обнаруживаются у различных животных, в почве, воде и продуктах питания. 7-12% взрослых были ранее инфицированы МАС, хотя частота заболевания варьирует в различных географических регионах.
Инфицирование происходит при ингаляции или инокуляция МАС через респираторный или гастроинтестинальный (часто при употреблении некипяченой воды) тракт.
Хотя MAC можно обнаружить в мокроте и кале у лиц, у которых нет клинических проявлений инфекции (носителей), инфекция развивается только при тяжелом иммунодефиците с числом лимфоцитов CD4 < 50 клеток/мкл (Horsburgh, 1999).
Другие факторы, которые ассоциированы с повышенным риском МАС-инфекции — высокая вирусная нагрузка (РНК ВИЧ > 100 000 копий/мл), предшествующие ОИ (особенно ЦМВИ), предшествующая колонизация респираторного или гастроинтестинального тракта МАС, и редукция in vitro лимфопролиферативного иммунного ответа на M. аvium антиген.
Не выявлено факторов внешней среды или образа жизни тесно ассоциированных с последующим развитием МАС-инфекции у предрасположенных пациентов.
Показано, что наиболее часто МАС-инфекция с поражением легких возникает у пациентов с гастроэзофагеальной рефлюксной болезнью, получающих кислотоснижающую терапию, что дает возможность микроорганизмам выживать в условиях кислой среды желудка.
Изолировать больных нет необходимости. Домашние или тесные контакты с больным МАС не имеют повышенного риска инфицирования и передача от человека к человеку маловероятна.
До появления эффективной АРТ и химиопрофилактики, диссеминированная МАС-инфекция развивались у 20-40% больных на стадии СПИД (Nightingale, 1992). Для лиц с уровнем CD4< 100 клеток/мкл, которые получают эффективную профилактику или отвечают на АРТ со стабильным повышением CD4> 100-200 клеток/мкл частота составляет 2 случая на 100 человека-лет. С появлением АРТ инфекции, вызванные атипичными микобактериями, стали редкостью (Karakousis, 2004). Однако изменилось и их течение. Раньше они протекали в основном как хроническая диссеминированная инфекция и нередко сочетались с кахексией. Сегодня они чаще встречаются в очаговых формах и почти всегда связаны с синдромом восстановления иммунитета. Сегодня возможны такие проявления инфекции, которые никогда не встречались раньше.
Наиболее часто наблюдают заболевание, вызываемое Mycobacterium avium complex (этиологический агент > 95% случаев атипичного микобактериоза на стадии СПИД). После установления диагноза инфекции, вызванной данным возбудителем, более 50% больных умирают в течение 6-10 мес.
Не исключено, что даже частичное подавление вирусной нагрузки достаточно для восстановления специфического иммунного ответа против MAC (Havlir, 2000). В результате восстановления иммунитета возможно даже полное выздоровление (Aberg, 1998).
Клиника.
После колонизации MAC слизистых оболочек пищеварительного тракта и дыхательных путей следует генерализация инфекционного процесса с развитием бактериемии. Изолированное поражение пищеварительного тракта с развитием эзофагита, дуоденита, энтерита или колита наблюдается реже. Генерализация процесса сопровождается поражением лимфатических узлов брыжейки. При диссеминации инфекции в патологический процесс вовлекается печень, селезенка и другие органы ретикуло-эндотелиальной системы. При гистологическом исследовании в этих органах обнаруживают макрофаги и тканевые гистиоциты с большим количеством внутриклеточных микроорганизмов.
Клинический спектр поражений, вызываемых атипичными микобактериями, представлен.
Клинические проявления заболеваний, вызванных атипичными микобактериями
| Клинические проявления | Возбудители |
| Поражение легких | Mycobacterium avium complex Mycobacterium kansasii Mycobacterium chelonae Mycobacterium xenopi |
| Лимфадениты различной локализации | Mycobacterium avium complex Mycobacterium scrofulaceum |
| Поражение кожи | Mycobacterium marinum Mycobacterium fortuitum Mycobacterium chelonae Mycobacterium ulceranse |
| Диссеминированная инфекция | Mycobacterium avium complex Mycobacterium kansasii Mycobacterium chelonae Mycobacterium genovense Mycobacterium haemophilum |
Клинические проявления заболевания, вызванного MAC протекают наиболее тяжело, зависят от иммунного статуса пациентов.
У больных с количеством лимфоцитов CD4 > 200 клеток/мкл развиваются локализованные поражения, в том числе легких, проявляющееся повышением температуры тела, кашлем, увеличением шейных и надключичных лимфатических узлов. При рентгенографии ОГК обнаруживают инфильтративные изменения.
Другие локализованные проявления МАС-инфекции описаны более часто среди пациентов, которые получают или отвечают на АРТ. Очаговые синдромы включают лимфаденит, пневмонит, перикардит, остеомиелит, абсцессы кожи и мягких тканей, генитальные язвы или инфекцию ЦНС.
Локализация гнойного лимфаденита может быть любой (описаны абсцессы шейных, паховых и мезентериальных лимфоузлов, в некоторых случаях с образованием свищей). Лимфаденит нередко принимает затяжное течение, иногда даже, несмотря на хирургическое лечение. Любой абсцесс на фоне тяжелого иммунодефицита и восстановления иммунитета с высокой вероятностью указывает на инфекцию, вызванную атипичными микобактериями. В число распространенных очаговых инфекций входят также поражения кожи, остеомиелит (особенно позвонков) и гнойный артрит (описаны случаи артрита коленного сустава, суставов кисти).
При тяжелой иммуносупрессии развивается диссеминированная форма заболевания, в клинике которой преобладают симптомы поражения пищеварительного тракта — диарея, потеря массы тела, анорексия; общие симптомы — утомляемость, слабость, повышение температуры тела до фебрильной; гепато- и спленомегалия. У 25% больных с диссеминированной формой заболевания наблюдают поражение легких, при котором на рентгенограмме ОГК выявляют очаговые инфильтративные изменения в нижних долях, увеличение прикорневых лимфатических узлов.
Заболевание обычно начинается остро, с высокой температуры (высокие размахи температуры), ознобов, болей в грудной клетке и кашля с отделением умеренного количества вязкой мокроты; нередко отмечается кровохарканье и кровотечения. Затем появляются выраженная слабость, повышенная потливость ночью, быстро присоединяется одышка. Характерна кахексия. Лимфоузлы часто увеличены, однако в первую очередь обращают на себя внимание не их размеры, а количество (Gordin, 1997). Дифференциальный диагноз должен включать ТБ и лимфому. При УЗИ выявляется увеличение печени и селезенки.
В крови обычно обнаруживается повышение активности щелочной фосфатазы (ЩФ); этот симптом у больных с тяжелым иммунодефицитом с высокой вероятностью указывает на инфекцию, вызванную MAC. Эту инфекцию следует исключать и при появлении анемии. Цитопения, особенно анемия, нередко указывает на поражение костного мозга.
Наиболее характерные клинические и лабораторные признаки диссеминированной МАС-инфекции представлены.
Наиболее характерные клинические и лабораторные признаки диссеминированной МАК-инфекции
| Клинические признаки | — лихорадка — отмечается почти у всех больных и может достигать очень высоких цифр (до 41-42 0С); — ночные поты — наблюдаются почти так же часто, как и лихорадка; — уменьшение массы тела; диарея, боли в животе могут быть обусловлены непосредственным поражением стенки кишечника микобактериями; — лимфаденопатия, гепатоспленомегалия. |
| Лабораторные признаки | — анемия, при которой требуются гемотрансфузии; — снижение показателя гематокрита; — повышение активности ЩФ; |
Симптомы диссеминированной инфекции, вызванной MAC, обычно неспецифичны. При лихорадке, потере веса и диарее у больных с числом лимфоцитов CD4 < 100 клеток/мкл всегда нужно исключать инфекцию, вызванную атипичными микобактериями.
Диагностика.Диссеминированную MAC-инфекцию нередко бывает трудно диагностировать. Материал для исследования нужно брать из всех очагов инфекции.
При подозрительной клинической симптоматике проводят посев крови на микобактерии. Посев крови на специальные среды служит основным методом диагностики инфекций, вызванных MAC. У большинства больных с клиническими проявлениями инфекции интенсивность микобактериемии такова, что возбудитель обнаруживается в большинстве (86-98%) или во всех посевах крови. Хотя MAC обычно растут быстрее, чем M.tuberculosis, получение результатов посева и исключение ТБ может занять несколько недель.
Поскольку при диссеминированной инфекции часто поражаются печень и костный мозг, микобактерии можно обнаружить в окрашенных на КУБ препаратах, приготовленных из биоптатов этих органов. Проводятся также посевы материала, полученного при биопсии. При анемии в диагностике часто помогает пункция костного мозга.
Также делают посев кала. Значение мокроты невелико. Если MAC обнаруживается в кале, мокроте или жидкости, полученной при БАЛ, инфекцию, требующую лечения, бывает трудно отличить от простой колонизации слизистых. В этих случаях, если общих симптомов нет, лечение начинать не следует. Такая же тактика относится и к Mycobacterium kansasii (Kerbiriou, 2003).
В материале, полученном из абсцессов, возбудитель обнаруживается почти всегда.
Предварительный диагноз заболевания устанавливают на основании клинической картины и выявления микобактерий в мазках кала, мокроты, окрашенных по Цилю-Нильсену, или препаратах, приготовленных из пунктата костного мозга, биоптатов печени или лимфатических узлов.
Лечение МАС-инфекции у детей.
Лечение МАС-инфекции у детей включает комплексную химиотерапию ципрофлоксацином, рифабутином и кларитромицином и проводится независимо от возраста. Жидких лекарственных форм рифабутина нет, однако суспензию можно приготовить самостоятельно: содержимое капсулы развести в вишневом или сахарном сиропе (10 мг/мл).
Схема лечения представлена. Курс антибактериальной терапии составляет 6 месяцев.
Лечение диссеминированных инфекций, вызванных атипичными микобактериями у детей
| Противомикробный препарат | Доза | Частота приема | Способ применения |
| Ципрофлоксацин + | 30 мг/кг | 2 раза в сутки (макс.доза 750 мг) | внутрь |
| Рифабутин + | 10-20 мг/кг | 1 раз в сутки (макс.доза 300 мг/сут) | внутрь |
| Кларитромицин | 7,5 мг/кг | 2 раза в сутки (макс.доза 550 мг) | внутрь |
Вторичная профилактика МАС-инфекции.
Вторичная профилактика необходима всем пациентам, леченным по поводу МАС-инфекции. Проводится теми же препаратами и в тех же дозах, что и для первичной профилактики (табл.18). Вторичная профилактика может быть прекращена у пациентов, которые получают ее > 12 мес. и имеют стабильный (сохраняющийся более 3-6 мес.) рост CD4 > 100 клеток/мкл.
Первичная медикаментозная профилактика МАС-инфекции.
Первичная профилактика МАС-инфекции начинается при уровне CD4 < 50 клеток/мкл. Проводится азалидами, макролидами или рифампицином (рифабутином). Препараты и дозы для первичной профилактики МАС-инфекции у взрослых и детей представлены в табл.12.
Первичная профилактика МАС-инфекции: препараты и дозы
| Препарат | Доза | ||
| для взрослых | для детей | ||
| Препарат выбора | азитромицин | 1200 мг внутрь 1 раз в неделю | 20 мг/кг 1 раз в неделю (максимальная доза 600 мг) |
| Альтернативный препарат | кларитромицин | по 500 мг внутрь 2 раза/сут | |
Профилактика может быть прекращена без какого либо риска, если в результате проведения АРТ уровень CD4 вырос > 100 клеток/мкл и сохраняется на таком уровне в течение 3 месяцев.
Источник
Электронный научный журнал
Современные проблемы науки и образования
ISSN 2070-7428
«Перечень» ВАК
ИФ РИНЦ = 0,931
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Хорошилова Н.Е. 1 Великая О.В. 1 Лушникова А.В. 1 Бородина И.В. 2
1 ФГБОУ ВО «Воронежский государственный медицинский университет им. Н.Н. Бурденко Минздрава России»
2 КУЗ ВО «Воронежский областной клинический противотуберкулезный диспансер им. Н.С. Похвисневой»
Во многих странах мира борьба с туберкулезной инфекцией остается важной задачей и нерешенной проблемой. В последнее время эпидемиологическая ситуация по туберкулезу улучшилась, но большой проблемой во фтизиатрии стал рост числа больных с сочетанной патологией туберкулеза и ВИЧ-инфекции. В Российской Федерации у лиц, живущих с ВИЧ-инфекцией, регистрируются не только случаи туберкулеза. Отмечается увеличение доли больных с достаточно редким инфекционным заболеванием — микобактериозом. Это группа заболеваний, вызываемых нетуберкулезными микобактериями (НТМБ), которые являются условно-патогенными микобактериями и вызывают развитие заболевания при определенных условиях (снижении иммунитета). Таким образом, микобактериоз — это оппортунистическое заболевание, которое развивается при определенной стадии ВИЧ-инфекции. В Российской Федерации на сегодняшний день не разработаны клинические рекомендации по ведению пациентов с микобактериозами, нет определенных нормативных документов для проведения диагностики и лечения данной категории больных, не существует принятой клинической классификации этого заболевания. Имеющиеся данные об этиологической структуре, эпидемиологии, клинике, диагностике микобактериозов достаточно скудны ввиду того, что увеличение количества больных микобактериозами связано с нарастающей волной больных ВИЧ-инфекцией. В статье представлены данные историй болезни двух пациенток с ВИЧ-инфекцией, которые были направлены в противотуберкулезный диспансер с подозрением на туберкулез легких. В результате дообследования туберкулез органов дыхания не подтвердился, а был установлен диагноз «микобактериоз легких».
туберкулез
микобактериоз
нетуберкулёзные микобактерии
ВИЧ-инфекция
1. Корнилова З.Х., Луконина И.В., Алексеева Л.П. Туберкулез в сочетании с ВИЧ-инфекцией // Туб. 2010. №3. С.3-9.
2. Оттен Т.Ф. Микобактериоз у больных с ВИЧ-инфекцией / В кн.: Беляков Н.А., Рахманова А.Г.(ред.). Вирус иммунодефицита человека-медицина. Гл.10.2. СПб.: Балтийский медицинский образовательный центр, 2011. С.199-224.
3. Великая О.В., Барковская Л.В., Хорошилова Н.Е., Лушникова А.В. Туберкулез и ВИЧ-инфекция в Воронежской области // Системный анализ и управление в биомедицинских системах. 2017. Т. 16, №3. С. 708-711.
4. Adjemian J., Prevots D. R., Gallagher J. et al. Lack of adherence to evidence based treatment guidelines for nontuberculous mycobacterial lung disease. Ann. Am. Thorac. Soc. 2014. V. 11, № 1. Р. 9-16.
5. Andréjak C., Nielsen R., Thomsen V. et al. Chronic respiratory disease, inhaled corticosteroids and risk of non-tuberculous mycobacteriosis. Thorax. 2013. V. 68, № 3. Р. 256-262.
6. Brode S.K., Daley C.L., Marras T.K. The epidemiologic relationship between tuberculosis and non-tuberculous mycobacterial disease: a systematic review. Int. J. Tuberc. lung Dis. 2014. V. 18, № 11. Р. 1370-1377.
7. Daley C. L., Griffith D. E. Pulmonary non-tuberculous mycobacterial infections. Int. J. Tuberc. Lung. Dis. 2010. V. 14, № 6. Р. 665-671.
8. Griffith D. E., Aksamit T., Brown-Elliott B. A. et al. An official ATS/ IDSA ement: Diagnosis, treatment, and prevention of nontuberculous mycobacterial diseases. Am. J. Respir. Crit. Care Med. 2007. V. 175, № 4. Р. 367-416.
Во многих индустриально развитых странах в последнем десятилетии наблюдается рост числа больных микобактериозами. Особую актуальность эта проблема приобрела в условиях распространения ВИЧ-инфекции. В последние годы и в России среди больных ВИЧ-инфекцией тоже нарастает регистрация случаев микобактериозов, вызванных нетуберкулезными микобактериями. Проблема микобактериозов актуальна не только для ВИЧ-инфицированных, но и для других категорий больных с иммунодефицитом. Микобактериозы часто наблюдаются у больных с хроническими неспецифическими заболеваниями легких, силикозом, раком легкого. У больных с иммунодефицитом, как правило, микобактериоз носит диссеминированный характер и в значительном числе случаев приводит к смерти. Повсеместное нарастание микобактериозов в настоящее время связано с увеличением числа больных с поражением иммунной системы, с хроническими неспецифическими заболеваниями легких, с ухудшением экологической обстановки, а также с улучшением диагностики. Это группа заболеваний, вызываемых нетуберкулезными микобактериями (НТМБ), которые являются условно-патогенными микобактериями и вызывают развитие заболевания при определенных условиях, чаще всего при снижении иммунитета. У лиц, живущих с ВИЧ-инфекцией, микобактериоз относится к оппортунистическим заболеваниям [1, 2]. Но, к сожалению, эпидемиологическая ситуация по сочетанной патологии туберкулеза и ВИЧ-инфекции ухудшается. В Воронежской области с 2000 г. наблюдается рост заболеваемости и распространенности туберкулеза у ВИЧ-инфицированных [3]. В Российской Федерации нет разработанных клинических рекомендаций для ведения пациентов с микобактериозами, не имеется определенных нормативных документов для проведения диагностики и лечения данной категории больных, нет принятой клинической классификации этого заболевания. Имеющиеся данные об этиологической структуре, эпидемиологии, клинике, диагностике микобактериозов достаточно скудны ввиду того, что увеличение количества больных микобактериозами связано с нарастающей волной больных ВИЧ-инфекцией. Согласно литературным данным микобактериозы встречаются во всех экономически развитых странах. В Северной Америке распространенность микобактериозов за период с 1998 по 2010 гг. была в пределах от 5,6 (США) до 9,8 (Канада) на 100 тыс. населения. В Южной Америке (только в Бразилии) с 1996 по 2005 гг. микобактериоз устанавливался в 1,0 случае на 100. тыс. населения случаев. В Европе заболеваемость колебалась от 0,6 до 1,7 случаев на 100 тыс. населения в 1992-2010 гг., но в Шотландии заболеваемость микобактериозом достигла величины 3,1 на 100 тыс. населения с 2005 по 2010 гг. А в Японии было зарегистрировано 938 случаев легочного микобактериоза с 1970 по 2003 гг. [4-7].
В настоящее время существуют руководство Американского общества по инфекционным болезням (IDSA) и руководство Американского торакального общества (АТS) «Диагностика, лечение и профилактика заболеваний, вызванных нетуберкулезными микобактериями», которые используют врачи во всем мире для диагностики, лечения и профилактики микобактериозов [8].
К клиническим и рентгенологическим критериям для постановки диагноза микобактериоза согласно рекомендациям относятся: имеющиеся респираторные симптомы; обнаружение при рентгенографическом исследовании в легких очаговых или полостных изменений или наличие при компьютерной томографии множественных бронхоэктазов с мелкими очагами, при этом должна быть проведена дифференциальная диагностика в целях исключения других заболеваний, имеющих сходную рентгенологическую картину.
К микробиологическим критериям микобактериоза относятся:
— наличие в двух и более независимо взятых образцах мокроты нетуберкулезных микобактерий;
— не менее одного положительного результата культурального исследования материала, полученного при проведении бронхоскопии (бронхоальвеолярный лаваж [БАЛ] или промывные воды бронхов);
или
— морфологические изменения в тканях и органах (наличие гранулематозного воспаления или обнаружение кислотоустойчивых бактерий) и наличие роста культуры НТМБ этой ткани или не менее из одного образца БАЛ / промывных вод бронхов или мокроты,
или все вышеперечисленные критерии. В настоящее время этот вопрос является дискуссионным и широко обсуждается.
Цель исследования — изучить особенности клинических проявлений и диагностики микобактериозов у лиц, живущих с ВИЧ-инфекцией.
Материал и методы исследования. Проведен анализ клинических проявлений и диагностики микобактериозов у лиц, живущих с ВИЧ-инфекцией. Представлены данные историй болезни двух пациентов с ВИЧ-инфекцией, которые были направлены в противотуберкулезный диспансер с подозрением на туберкулез легких. В результате дообследования туберкулез не подтвердился, а был установлен диагноз «микобактериоз».
Результаты исследования и их обсуждение
Клиническое наблюдение 1
Пациентка Ш. (35 лет). Туберкулезом раньше не болела. Наблюдалась в Центре по борьбе со СПИД в течение 10 лет (4В стадия), получала антиретровирусную терапию. В июле 2018 г. перенесла пневмоцистную пневмонию, лечилась в стационаре, выписана с улучшением. В начале ноября состояние вновь ухудшилось, госпитализирована в стационар Центра по борьбе со СПИД. При обследовании на рентгенограмме легких выявлена патология, в мокроте обнаружены кислотоустойчивые микобактерии (КУМ), в связи с чем переведена в противотуберкулезный диспансер (ПТД) для исключения туберкулеза.
При поступлении в ПТД 22.11.2018 жалобы на кашель со слизистой мокротой до 50 мл в сутки, одышку при незначительной физической нагрузке, слабость, повышение температуры тела до 37оС, похудение на 4 кг за последний месяц. Общее состояние средней тяжести, пониженного питания, кожные покровы бледные. Дыхание жесткое с бронхиальным оттенком, гудящие хрипы в нижних отделах легких. ЧДД 24 в минуту. АД 90/55 мм рт. ст. Печень выступает на 7 см из-под подреберья.
Общий анализ крови: гемоглобин — 75 г/л; эритроциты — 2,9х1012/л; цветной показатель — 0,75; лейкоциты — 15,4х109/л; эозинофилы — 1; палочкоядерные — 16; сегментоядерные — 74; лимфоциты — 3; моноциты — 6; СОЭ — 57 мм/ч.
Общий анализ мочи: удельный вес — 1024; белок — 0,3; эритроциты — 1-2; лейкоциты — 5-6; цилиндры — 3-4.
Количество СD4+ лимфоцитов — 42 клетки/мкл.
В мокроте методом люминесцентной микроскопии выявлены кислотоустойчивые микобактерии КУМ (+) от 21.11.2018, 23.11.2018, 27.11.2018.
В мокроте методом ПЦР РВ от 26.11.2010 ДНК МБТ не выявлены; ПЦР Дженэксперт от 23.11.2018 ДНК МБТ не выявлены.
В мокроте посевом (BACTEC) от 23.11.2018, 26.11.2018 НТМБ(+). Иммунохроматографический тест на микобактерии туберкулеза TBAgMRT64 Rapid — отрицательный. Реакция на Диаскинтест отрицательная.
УЗИ органов брюшной полости: УЗ-признаки гепатоспленомегалии, диффузных изменений печени и поджелудочной железы.
Фибробронхоскопия: слева бронхи без особенностей. В просвете среднедолевого бронха (СДБ) справа густая слизисто-гнойная мокрота. По задней стенке СДБ с переходом на латеральную изъязвление, дно которого покрыто густыми массами белого цвета. Вокруг слизистая отечна, гиперемирована. Множество бугорков. За счет этих изменений БС4 сужено почти наполовину. Выше слизистая незначительно отечна. Шпора СДБ острая.
Гистологическое исследование биопсийного материала: в биоптате мелкие кусочки некротического детрита и фрагменты неспецифической грануляционной ткани с диффузной лимфоцитарной и нейтрофильной инфильтрацией, обилие мелких кровеносных сосудов.
При окраске по Цилю-Нильсену КУМ не определяются.
Заключение: морфологическая картина неспецифического воспаления.
На обзорной рентгенограмме органов грудной клетки в прямой и правой боковой проекции определяются массивное неоднородное инфильтративное затенение в средней доле правого легкого с четкой границей по междолевой борозде, неоднородное инфильтративное затенение в проекции 9-го сегмента левого легкого. Корни расширены. Тень средостения смещена влево (рис. 1, 2).
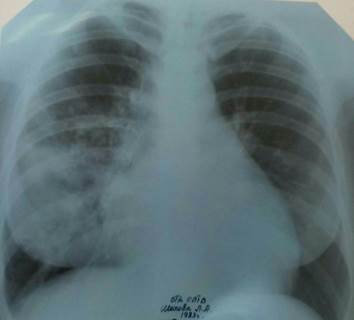
Рис. 1. Обзорная рентгенограмма органов грудной клетки в прямой проекции больной Ш.
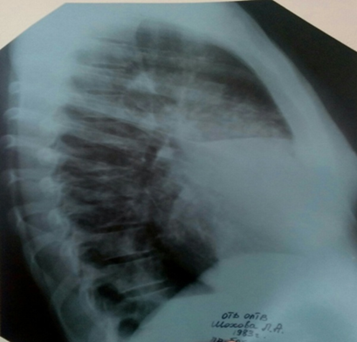
Рис. 2. Обзорная рентгенограмма органов грудной клетки в правой боковой проекции больной Ш.
Мультиспиральная компьютерная томография органов грудной полости: в верхних и средних долях правого легкого массивная инфильтрация, участки консолидации в S8 нижней доли. Множественные полиморфные очаги по всем полям, больше справа. Часть из них с деструкцией. Лимфатические узлы гиперплазированы до 12-14 мм. Сердце обычных размеров, в перикарде жидкость, толщина слоя 12 мм. Дегенеративные изменения позвоночника. Костно-деструктивных изменений не выявлено.
Диагноз «микобактериоз» был установлен на основании обнаружения НТМБ в двух образцах мокроты методом посева, данных биопсийного материала, отрицательных результатов молекулярно-генетических методов, иммунохромотографического теста на МБТ.
Таким образом, у больной были типичные клинические проявления микобактериоза: кашель, одышка, лихорадка, потеря веса, анемия. Имелись рентгенологические изменения в легких в виде фокусов и очагов и поражение внутригрудных лимфатических узлов. Диагноз верифицирован бактериологическим методом исследования мокроты (рост НТМБ в двух анализах мокроты методом ВАСТЕК).
Клиническое наблюдение 2
Пациентка М., 32 года. Из анамнеза известно, что туберкулезом раньше не болела, наблюдается в Центре по борьбе со СПИД с 2008 г. (4В стадия), получает автиретровирусную терапию (АРВТ). В августе 2018 г. перенесла менингоэнцефалит. Состояние ухудшилось в октябре 2018 г., когда стали беспокоить кашель, общая слабость, плохой аппетит. Была госпитализирована в стационар. В легких при рентгенологическом исследовании выявлена патология. Больной была назначена антибактериальная терапия. При исследовании мокроты получили КУМ(+) методом люминесцентной микроскопии. Для исключения туберкулеза пациентка направлена в противотуберкулезный диспансер.
При поступлении в противотуберкулезный диспансер: состояние относительно удовлетворительное. Кожные покровы чистые, бледные. В легких дыхание аускультативно жесткое, хрипы не выслушиваются. ЧДД — 18 в минуту. Тоны сердца ритмичные ЧСС — 78 ударов в минуту, АД 100/65 мм рт. ст. Язык влажный, с белым налетом. Живот мягкий, безболезненный.
Общий анализ крови от 28.11.2018: гемоглобин — 130 г/л; эритроциты — 3,8х10/л; цветной показатель — 1,0; лейкоциты — 8,5х109/л; эозинофилы — 2%; палочкоядерные — 3%; сегментоядерные — 76%; лимфоциты — 8%; моноциты — 11%; СОЭ — 33 мм/ч.
Общий анализ мочи от 28.11.2018: уд. вес — 1020; белок — 0,19 г/л; лейкоциты — 1-3 в поле зрения.
Количество СD4+ лимфоцитов 101 клетка/мкл от 27.11.2018.
В мокроте КУМ (+) от 28.11.2018, 05.12.2018, 06.12.2018, 14.12.2018, 18.12.2018 методом люминесцентной микроскопии.
В мокроте методом ПЦР-РВ от 04.12.2018, 20.12.2018 ДНК МБТ не выявлены.
ПЦР Дженэксперт от 03.12.2018 ДНК МБТ не выявлены.
В мокроте посевом (BACTEC) от 05.12.2018, 06.12.2018 НТМБ(+). Иммунохроматографический тест на МБТ TBAgMRT64 Rapid — отрицательный.
Реакция на Диаскинтест — отрицательная.
Фибробронхоскопия № 1: слева устье нижнедолевого бронха сужено до почти щелевидного за счет бугристой опухоли с густым налетом некроза белого цвета.
Биопсия № 1: в собственном слое слизистой обилие мелких кровеносных сосудов и диффузная воспалительная инфильтрация лимфоидного и нейтрофильного характера, на фоне которого определяются мелкие нечеткие эпителиоидно-клеточные гранулемы. При окраске по Цилю-Нильсену КУМ не определяются.
Фибробронхоскопия № 2: устье верхнедолевого бронха справа полностью стенозировано бугристой опухолью с густым налетом фибрина белого цвета.
Биопсия № 2: в биоптате — мелкие фрагменты слизистой, местами покрытые многослойным плоским эпителием, местами — слоем некротического детрита. В слизистой — диффузная нейтрофильная и лимфоцитарная инфильтрация, на фоне которой местами определяются нечеткие мелкие эпителиоидно-клеточные гранулемы. В центре некоторых гранулем — скопление ядерного детрита. При окраске по Цилю-Нильсену КУМ не обнаружены.
МСКТ ОГК: в верхней доле S1, S2 справа и нижней доле S6 и базальной пирамиде левого легкого определяются очаговые изменения, деструкция четко не видна. Гиперплазированы бронхопульмональные лимфатические узлы. Средостение структурно не смещено.
В представленном случае клинические проявления микобактериоза (кашель, общая слабость, потеря веса) были мало выраженными. Это можно объяснить количеством СД4+ лимфоцитов (101 кл/мкл). Диагноз микобактериоза поставлен своевременно благодаря бактериоскопическому исследованию мокроты больной, консультации фтизиатра и комплексу обследований в противотуберкулезном диспансере.
Выводы
1. В настоящее время наблюдается рост заболеваемости микобактериозами у лиц, живущих с ВИЧ-инфекцией. Для своевременного выявления микобактериозов у врачей различных специальностей должна быть настороженность.
2. Диагноз микобактериоза следует устанавливать на основании комплексного клинико-рентгенологического и микробиологического обследования. Главными критериями при постановке данного диагноза должны быть выделение культуры НТМБ и гистологическая верификация.
Библиографическая ссылка
Хорошилова Н.Е., Великая О.В., Лушникова А.В., Бородина И.В. МИКОБАКТЕРИОЗ У ЛИЦ, ЖИВУЩИХ С ВИЧ-ИНФЕКЦИЕЙ: ДВА КЛИНИЧЕСКИХ НАБЛЮДЕНИЯ // Современные проблемы науки и образования. — 2019. — № 6.;
URL: https://science-education.ru/ru/article/view?id=29441 (дата обращения: 20.05.2021).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник